Cosa sappiamo della risposta immunitaria contro il COVID-19? Dopo essere stati infettati dal SARS-CoV-2, rimaniamo immuni al virus? Perché alcune persone vengono reinfettate? Un vaccino potrebbe risolvere una volta per tutte la pandemia? In questo articolo proveremo a rispondere a queste e altre domande, in base allo stato attuale delle conoscenze.
La risposta immunitaria
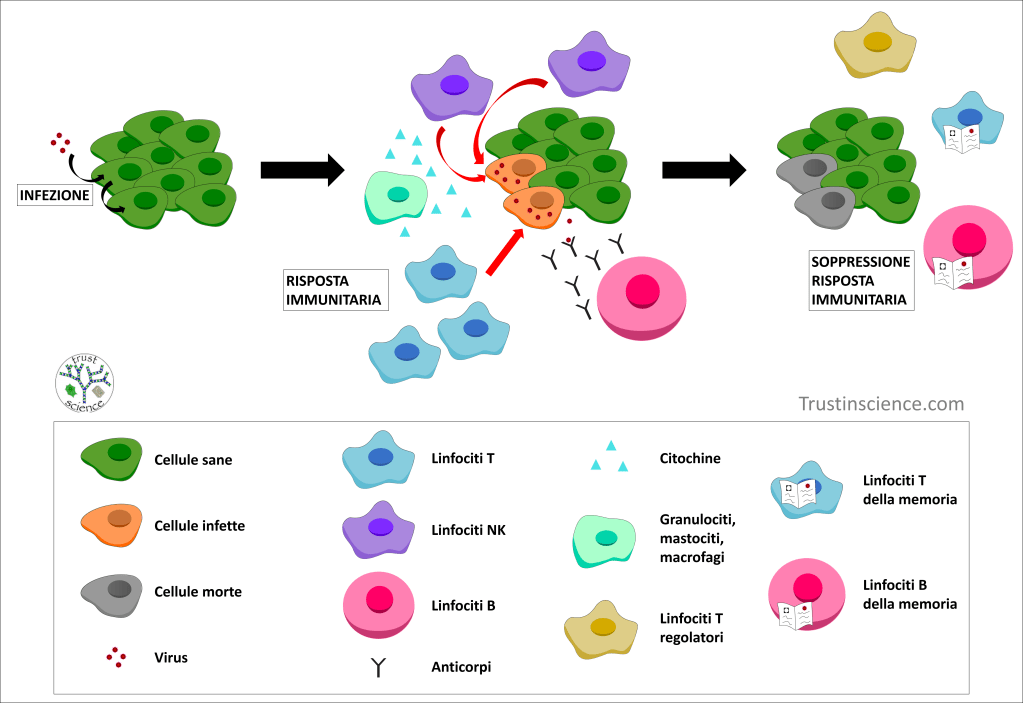
Quando un agente patogeno (virus, batteri, parassiti) entra nell’organismo, provoca un’infezione. In risposta a ciò, le cellule del sistema immunitario (chiamate leucociti o globuli bianchi) danno inizio ad un processo infiammatorio. Il sistema immunitario si distingue in innato e adattativo. Il primo offre una risposta immediata e non specifica contro il patogeno; il secondo invece richiede prima la sua identificazione e poi fornisce una risposta più forte e specifica, garantendo anche la memoria immunologica. Grazie a quest’ultima, in caso di reinfezione perpetrata dal medesimo agente patogeno, l’organismo reagirà con una forte risposta immunitaria, specifica ed immediata.
Fanno parte del sistema immunitario innato i linfociti NK (Natural Killer), i mastociti, i granulociti, i macrofagi e le cellule dendritiche. I granulociti e i mastociti intervengono nella fase iniziale della risposta infiammatoria, rilasciando alcune molecole che sono tossiche per i batteri e altre che chiamano i rinforzi. Queste ultime si chiamano citochine e sono necessarie per iniziare e poi mantenere la risposta infiammatoria. Un sottogruppo di granulociti condivide insieme ai macrofagi la capacità di eliminare dall’organismo particelle estranee (frammenti di agenti patogeni, ad esempio). I linfociti NK uccidono le cellule che sono state infettate senza però essere in grado di riconoscere l’agente patogeno, mentre le cellule dendritiche raccolgono frammenti del patogeno e li presentano ai linfociti T, per attivare la risposta immunitaria adattativa.
Tra le cellule del sistema immunitario adattativo distinguiamo i linfociti B e i linfociti T (che si distinguono a loro volta in CD4+ e CD8+).
I linfociti B sono deputati alla produzione di anticorpi e alcuni di essi, al termine dell’infezione diventano linfociti B della memoria, che intervengono prontamente in caso di reinfezione da parte del patogeno contro il quale hanno sviluppato gli anticorpi.
I linfociti T CD8+ determinano una risposta citotossica, uccidendo le cellule infette dal virus. Questa funzione è condivisa con i linfociti NK, anche se viene svolta con un meccanismo differente, dal momento che i T CD8+ sono in grado di riconoscere il patogeno responsabile dell’infezione e quindi di offrire una risposta più specifica ed efficace. Quando l’infezione viene risolta, la maggior parte dei linfociti T CD8+ viene eliminata. Tuttavia, alcune cellule sopravvivono e diventano linfociti T della memoria, per offrire una risposta rapida ad una eventuale riesposizione al medesimo patogeno (come i linfociti B della memoria).
La maggior parte dei linfociti T CD4+ (chiamati T helper) svolge la funzione di coadiuvante, incrementando l’attività dei linfociti B e T CD8+. Altri invece, chiamati linfociti T regolatori, sopprimono la risposta immunitaria quando questa non è più necessaria: infatti, una risposta immunitaria eccessiva diventa dannosa per l’organismo, in quanto i globuli bianchi possono avere un effetto tossico anche sulle cellule sane (come nel caso delle malattie autoimmuni). Per evitare che ciò si verifichi, questo tipo di linfociti agisce come un “freno immunitario” che spegne il processo infiammatorio quando l’infezione viene eliminata.
Risposta immunitaria e COVID-19
Questa introduzione era doverosa per comprendere cosa succede quando il coronavirus SARS-CoV-2 infetta le cellule dell’epitelio delle vie aeree. Il virus inizia a replicarsi all’interno delle cellule, che in risposta attivano una procedura di morte programmata per contrastare la diffusione dell’infezione. In questo modo, frammenti del virus vengono rilasciati nell’ambiente circostante e sono poi raccolti dalle cellule dendritiche. L’organismo reagisce scatenando una risposta infiammatoria, che attira al sito dell’infezione i linfociti T e altre cellule dell’immunità innata. Mentre le cellule dell’immunità innata iniziano la loro risposta infiammatoria aspecifica, inizia il processo di identificazione del virus da parte dei linfociti T CD4+. Quando il patogeno viene identificato, le cellule B iniziano a produrre anticorpi in grado di contrastare le particelle virali. Gli anticorpi coadiuvano poi la risposta citotossica specifica dei linfociti T CD8+, che si aggiunge a quella aspecifica dell’immunità innata.
Una scoperta interessante è che nei casi più gravi di COVID-19, il “freno immunitario” dei linfociti T regolatori sembra non intervenire per spegnere la risposta infiammatoria. I ricercatori hanno scoperto che i polmoni di pazienti gravi con COVID-19 accumulano una vasta gamma di linfociti T iperattivi, suggerendo che il meccanismo di controllo non entri in funzione. Questa reazione eccessiva impedisce all’organismo di combattere efficacemente il virus, oltre a causare ulteriori danni ai polmoni, provocando una grave infiammazione e la distruzione dei tessuti sani (si veda l’immagine sottostante). Il termine medico per indicare questo fenomeno è “tempesta di citochine“. Quando il “freno immunitario” non funziona, le citochine continuano ad essere prodotte, mantenendo l’infiammazione attiva anche quando non più necessaria.
Un’altra scoperta interessante nei casi gravi di COVID-19 è la linfocitopenia, ovvero una diminuzione dei linfociti T e B nel sangue durante la malattia. La linfocitopenia è stata osservata anche in infezioni provocate da altri virus respiratori, come l’influenza, ma sembra che quella legata al COVID-19 sia più marcata e duri più a lungo.
In apparenza ci troviamo davanto ad una situazione paradossale: com’è possibile che la quantità di linfociti diminuisca e allo stesso tempo si verifichi un “eccesso di risposta immunitaria”? La spiegazione risiede nello squilibrio che si verifica nel sistema immunitario. Nei pazienti più gravi affetti da COVID-19, è stata notata una marcata diminuzione del numero di linfociti T (tutti i sottogruppi), B e NK. Allo stesso tempo, è stato misurato un aumento del numero di granulociti e macrofagi, ovvero i responsabili del rilascio di citochine infiammatorie. Questo squilibrio impedisce ai linfociti T regolatori di spegnere la risposta infiammatoria, che pertanto continua ad oltranza.

Memoria immunologica: sì o no?
Studi preliminari suggeriscono che gli anticorpi nelle persone infette da SARS-CoV-2 diminuiscano in modo significativo entro 2-3 mesi dall’infezione, suscitando la preoccupazione che l’immunità contro il virus possa scemare rapidamente e mettendo quindi in dubbio l’utilità di un vaccino. Tuttavia, è normale che i livelli di anticorpi diminuiscano dopo l’eliminazione di un’infezione. Ad esempio, per quanto riguarda le infezioni stagionali da coronavirus (per esempio quelli che provocano i banali raffreddori), in genere gli anticorpi iniziano a diminuire circa una settimana dopo l’infezione e rimangono in circolo per massimo un anno. È inoltre importante ricordare che i linfociti B e T della memoria si formano dopo l’infezione e possono essere riattivati quando lo stesso virus si ripresenta nell’organismo una seconda volta, per prevenire una nuova infezione. Dati preliminari (e quindi non ancora confermati oltre ogni ragionevole dubbio, per dirla alla Law and Order) suggeriscono che le cellule della memoria siano presenti nei pazienti guariti da sintomi lievi di COVID-19 diverso tempo dopo l’infezione. Questo rinvigorisce la speranza che un vaccino possa garantire un’immunità a lungo termine.
I linfociti T della memoria specifici per il coronavirus SARS-CoV-2 sono stati rilevati anche in individui “asintomatici esposti al virus” (parenti di casi confermati) che erano risultati negativi al test per gli anticorpi, suggerendo un’infezione asintomatica. Uno studio ha dimostrato che circa il 93% degli individui “asintomatici esposti” ha sviluppato una risposta al virus, nonostante gli anticorpi siano stati rilevati solo nel 60% dei casi. Le infezioni asintomatiche possono quindi essere più comuni di quanto ipotizzato e il solo test degli anticorpi può sottostimare la reale prevalenza dell’infezione o il grado di immunità della popolazione. I linfociti T della memoria specifici per SARS-CoV-2 sono stati trovati anche nella maggior parte dei pazienti convalescenti, il che lascia ben sperare che l’infezione (e quindi il vaccino) possa portare all’immunità.
Reinfezione
Il 12 ottobre 2020, su The Lancet Infectious Diseases, Richard L Tillett e colleghi hanno descritto il primo caso confermato di reinfezione da SARS-CoV-2 negli Stati Uniti. Un uomo di 25 anni del Nevada, che non aveva disturbi immunitari noti, contrasse un’infezione da SARS-CoV-2 nell’aprile 2020. Dopo essere guarito, risultò negativo a due test successivi. Tuttavia, 48 giorni dopo il primo test, il paziente è risultato nuovamente positivo al virus. Il sequenziamento del genoma virale ha mostrato che entrambe le infezioni erano state provocate da virus appartenenti allo stesso ceppo, ma che si trattava di due eventi distinti.
Finora sono documentati solo 4 casi di reinfezione: oltre all’individuo appena citato, si aggiungono un uomo di 33 anni di Hong Kong, un uomo di 46 anni dell’Ecuador e una donna di 51 anni del Belgio. È plausibile che il numero di casi sia maggiore, essendo questi noti solo per la sintomatologia importante della reinfezione: se la presenza di anticorpi generati durante la prima infezione ha permesso il decorso asintomatico della seconda, questa non viene registrata.
Al momento le informazioni disponibili sono insufficienti per trarre conclusioni. Finora non vi sono indicazioni per cui le reinfezioni siano dovute all’evasione immunitaria (ovvero che il virus sia stato in grado di eludere gli anticorpi già presenti), ragion per cui si ipotizza che un vaccino sarà sufficiente a conferire protezione contro tutte le varianti circolanti del virus.
Fonti
https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(20)30783-0/fulltext
